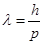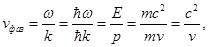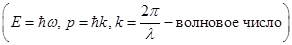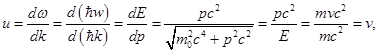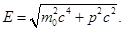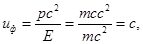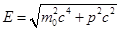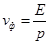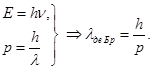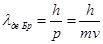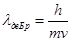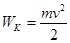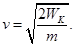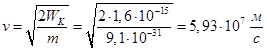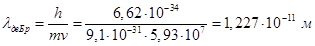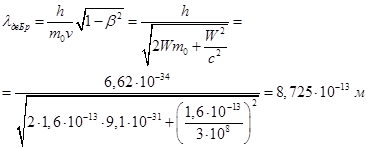Как определить длину волны де Бройля для электрона
Волна де Бройля или волна амплитуды вероятности
Волна де Бройля является волной вероятности или волной амплитуды вероятности, которая определяет плотность вероятности обнаружения объекта в конкретной точке конфигурационного пространства.
Согласно определения волн де Бройля, можно сделать вывод об их взаимодействии с какими-либо частицами и их волновой природе. Формулировка волн материи была введена в науку в 1924 году французским физиком-теоретиком Луи де Бройлем. Благодаря теории, свойство корпускулярно-волнового дуализма (или двойственности) было распространено на любые проявления материи, включая излучение и какие-либо частицы вещества.
В современной квантовой теории «волна материи» понимается несколько иначе. Однако название данного физического феномена, связанного с частицами вещества, включая водород, сформулировано в честь автора гипотезы.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
В 1913 году Н. Бор предложил полуклассическую модель атома, в основе которой было два постулата:
- Момент импульса электрона в атоме строго определен. Величина в любом случае пропорциональна nh/2π, где n – какое-либо целое число, начиная с 1, а h – постоянная Планка, присутствие которой в формуле ясно свидетельствует о том, что момент импульса частицы квантован. Таким образом, атом включает комплекс разрешенных орбит, по которым только и может перемещаться электрон. Когда электрон расположен на этих орбитах, излучение (то есть потеря энергии) отсутствует.
- Атомный электрон излучает или поглощает энергию в процессе перехода с одной орбиты на другую в количестве, определяемом, как разность энергий на этих орбитах. В связи с тем, что промежуточные состояния между разрешенными орбитами отсутствуют, излучение строго квантуется. Показатель его частоты составляет (E1 – E2)/h, что является выводом из формулы Планка для энергии E = hν.
Таким образом, боровская модель атома не предусматривает излучение электрона на орбите, его нахождение между орбитами. Однако согласно простой рассматриваемой модели, движение электрона рассматривают с классической точки зрения, как вращение планеты вокруг Солнца.
В процессе поиска ответа на вопрос о поведении электрона Де Бройль предположил, что электрону в любом случае должна соответствовать определенная волна. Благодаря ей, частица «выбирает» исключительно такие орбиты, на которых данная волна укладывается целое число раз. В этом и заключался смысл целочисленного коэффициента в постулированной Бором формуле.
Гипотеза приводит к выводу, что электронная волна де Бройля не является электромагнитной, а волновые параметры должны быть характерны для любых материальных частиц, а не только для электронов в атоме. Ученому удалось получить важное соотношение, с помощью которого можно определить тип этих рассматриваемых волновых свойств. Формула расчета волны де Бройля:
\(λ = h/p\)
где λ – является длиной волны, p – определяет импульс частицы в уравнении.
Де Бройль объединил в одном соотношении корпускулярную и волновую характеристики материи: такие, как импульс и длина волны. Данные параметры связывает постоянная Планка, величина которой примерно составляет \(6,626*10^{-27} эрг∙с\) или \(6,626*10^{-34} Дж∙с\), задающая масштаб проявления волновых свойств вещества.
Природа волн де Бройля, фазовая и групповая скорость
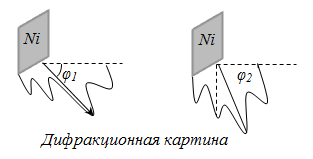
Следует отметить, что волны де Бройля, называемые электронными волнами, не являются электромагнитными. В 1927 году американским физикам Дэвиссону и Джермеру удалось подтвердить гипотезу де Бройля. Ученые обнаружили дифракцию электронов на кристалле никеля. В процессе получилось определить дифракционные максимумы, которые соответствуют формуле Вульфа-Брэггов:
\(2dsinj = nl\)
Расчет брэгговской длины волны подтвердил ее соответствие формуле:
В дальнейшем гипотеза де Бройля была подтверждена опытным путем Л.С. Тартаковским и Г. Томсоном. Ученым удалось зафиксировать дифракционную картину, когда пучок быстрых электронов при Е≈ 50 кэВ проходит сквозь фольгу из разных металлов.
Чуть позже получилось обнаружить дифракцию нейтронов, протонов, атомных пучков и молекулярных пучков. В дальнейшем были изобретены инновационные методики исследования вещества, включая нейтронографию и электронографию, сформировалось направление электронной оптики.
Макротела должны характеризоваться аналогичными свойствами. В случае, если m = 1кг, \(l = 6,62*10^{-31} м\) – невозможно обнаружить современными методами – поэтому макротела рассматриваются только в качестве корпускул.
В том случае, когда частица с массой m перемещается со скоростью v, фазовая скорость волн де Бройля будет определяться по формуле:
Исходя из того, что c > v, фазовая скорость волн де Бройля превышает скорость света в вакууме. Можно отметить, что фазовая скорость Vф может быть больше и может быть меньше с, в отличие от групповой скорости. Формула групповой скорости:
Таким образом, групповая скорость волн де Бройля соответствует скорости движения частицы. В случае фотона она будет равна:
В результате, значение групповой скорости равно скорости света.
Волны де Бройля подвержены дисперсии. Если подставить выражение:
в формулу:
получим следующее равенство:
\(Vф= f(λ)\)
Так как присутствует дисперсия, волны де Бройля невозможно представить, как волновой пакет. В противном случае, он мгновенно «расплывется», то есть исчезнет, в течение 10-26 с.
Какой формулой определяется длина волны
Количественные соотношения, которые связывают корпускулярные и волновые способности частиц, аналогичны свойствам фотонов:
Гипотеза де Бройля основана на универсальном характере данного равенства, что справедливо в условиях любых волновых процессов. Какой-либо частице, которая обладает импульсом р, соответствует волна. Ее длину можно определить с помощью формулы де Бройля:
p =mv- является импульсом частицы, h – определяется, как постоянная Планка.
Как определить длину волны де Бройля для электрона
Рассчитать длину волны де Бройля для электрона можно на конкретном примере. Предположим, то требуется определить длину волны де Бройля λ для электрона, кинетическая энергия которого составляет:
- W1 = 10 кэВ;
- W2 = 1 МэВ.
В первую очередь стоит записать исходные данные:
\(m_{e}=9,1*10^{-31} кг\)
\(W1 = 10 кэВ = 10*10^{3}*1,6*10^{-19} = 1,6*10^{-15}Дж\)
\(W2 = 1 МэВ = 10*10^{6}*1,6*10^{-19}= 1,6*10^{-13} Дж\)
Требуется найти λ.
Решение:
Формула волны де Бройля:
Так как известна кинетическая энергия электронов, можно рассчитать их скорость:
Далее можно определить длину волны де Бройля:
В том случае, когда скорость v частиц соизмерима со скоростью света с, длину волны де Бройля можно рассчитать по формуле:
Заметили ошибку?
Выделите текст и нажмите одновременно клавиши «Ctrl» и «Enter»
Нашли ошибку?
Текст с ошибкой:
Расскажите, что не так