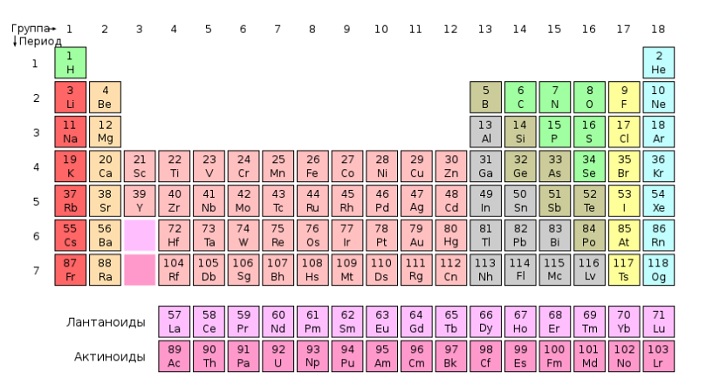
Периодическая таблица химических элементов Менделеева
Периодическая таблица: история
К середине XIX века было известно о 63 химических элементах. Химики всего мира боролись над созданием единой концепции, пытались объединить эти элементы в некую систему. Их предлагалось структурировать согласно возрастанию их атомной массы, а также разбить на группы по принципу схожести свойств.
В 1863 году Джон Александр Ньюленд опубликовал свой вариант схемы химических элементов. Однако его работу никто не принял всерьез, так как Ньюленд увлекался поиском связи между музыкой и химией.
В 1869 году Дмитрий Менделеев предложил свою схему периодической таблицы. Позже он ее не раз правил и улучшал, пока она не приняла привычный нам вид.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Суть открытия заключается в том, что рост атомной массы элементов влияет на химические свойства не монотонно, а периодически. После некоторого количества разных по свойствам элементов, свойства начинают повторяться. Так, калий схож с натрием, фтор — с хлором, а золото — с серебром и медью.
Через два года Менделеев окончательно объединил свои идеи, создал на их основе закон и предсказал открытие новых элементов. Позже ученые, отрывшие галлий, германий и скандий, подтвердили его догадки.
В современной формулировке закон звучит следующим образом: свойства элементов находятся в периодической зависимости от заряда их атомных ядер.
Структура таблицы
Таблица состоит из двух основных блоков:
- периодов;
- групп.
Горизонтальные строчки — периоды, вертикальные — группы.
В группах находятся элементы, которые схожи по своим химическим свойствам. В периодах же эти свойства постепенно изменяются.
Стоит отметить, что номер периода, в котором расположен элемент, соответствует номеру его валентной оболочки. Эта оболочка постепенно заполняется к концу периода.
Расположение элементов
В левой части таблицы находятся элементы, у которых ярко проявляются свойство восстановителя. Большая часть из них — металлы. Например, магний (Mg), кальций (Ca), натрий (Na), литий (Li).
В правой части расположены типичные неметаллы с окислительными свойствами. Например, кислород (O), хлор (Cl), фтор (F).
В середине собраны элементы, которые проявляют свойства как окислителя, так и восстановителя. Эти свойства проявляются по-разному в зависимости от того, с каким элементом они взаимодействуют. Ярким представителем является сера (S).
Несмотря на то, что элементы в периоде не сходятся по своим свойства, для всей таблицы есть важная закономерность: все периоды начинаются с активного металла, а заканчиваются инертным газом.
Свойства таблицы
Номер группы совпадает с числом валентных электронов, способных участвовать в образовании химических связей. Именно поэтому номер группы зачастую совпадает с валентностью.
Некоторые группы имеют свои названия. А именно:
- I — щелочные металлы;
- II — щелочноземельные металлы;
- III-V — нет группового названия;
- VI — халькогены;
- VII — галогены;
- VIII — благородные газы.
Также важной особенностью таблицы является то, что порядковый номер элемента совпадает с его ядерным зарядом.
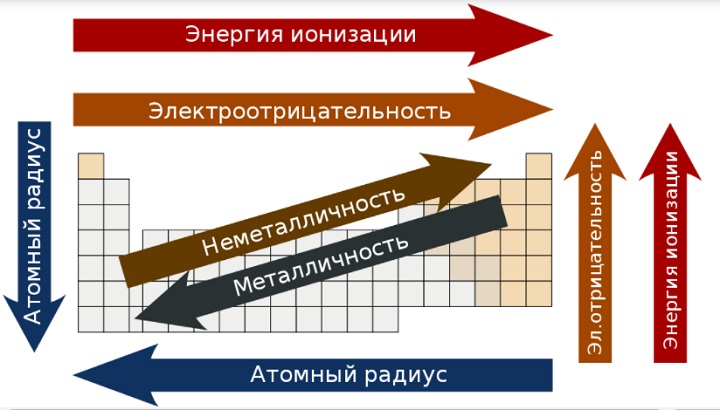
Основные закономерности системы Менделеева в форме таблицы. Стрелки указывают на увеличение значения того или иного показателя.
Последние изменения в таблице
В 2011 году таблица пополнилась на два элемента — флеровий и ливерморий, которые получили 114-й и 116-й атомные номера соответственно.
В 2016 году к ним добавились синтезированные учеными элементы с атомными номерами 113, 115, 117 и 118.
Открытие 113-го элемента принадлежит ученым из японского Института естественных наук. Элемент назван японием/ нихоний Nh.
115-й, 117-й и 118-й элементы открыла российско-американская команда ученых из Объединенного института ядерных исследований в Дубне, Ливерморской национальной лаборатории в Калифорнии и Окриджской национальной лаборатории в Теннесси. 115-ый элемент стал московием (Мс), 117-ый — теннессином (Тs), 118-ый — унуктонием (Оg).
Соответственно, сегодня Периодическая система химических элементов включает в себя 118 составляющих.
Заметили ошибку?
Выделите текст и нажмите одновременно клавиши «Ctrl» и «Enter»
Нашли ошибку?
Текст с ошибкой:
Расскажите, что не так