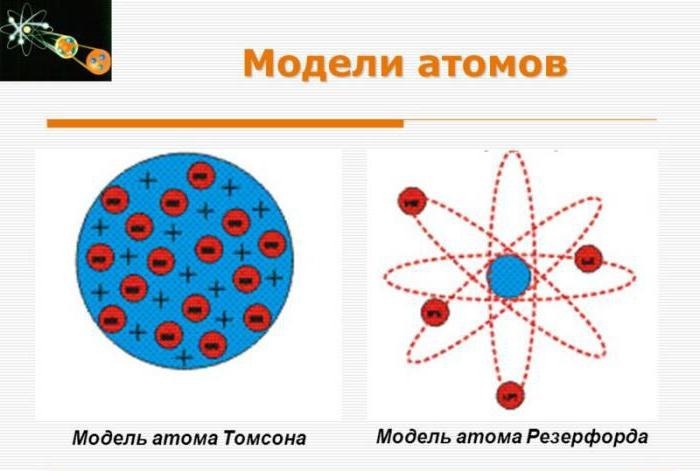
Строение планетарной модели атома Томсона: плюсы и минусы
Модель атома Томсона — что из себя представляет
Модель атома Томсона является одной из ранних моделей, описывающей строение атома, которая в дальнейшем была признана несостоятельной.
Рассматриваемая модель атома была представлена в 1904 году Д.Д. Томсоном. Открытию предшествовало обнаружение электронов, а после формулировки гипотезы было обнаружено атомное ядро.
Томсон выдвинул предположение о том, что атом является равномерно распределенным по всему объему зарядом со знаком плюс. Положительно заряженное «облако» содержит внутри небольшие электроны с отрицательным зарядом, расположение которых определено случайно.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Подобная модель напоминает пудинг с изюмом. Общий заряд атома нейтрален, что обусловлено равенством по модулю суммарного заряда электронов и заряда «облака». Данную модель нередко называют «пудинговой моделью атома».
Предыстория открытия, чем отличалась от модели Резерфорда
В физике 1897 год отмечен знаменательным событием. В это время Джозефом Джоном Томсоном были открыты электроны. Таким образом, ученому удалось экспериментальным путем подтвердить гипотезу о том, что атом – не «монолитная» частица. Вместе с тем отсутствовало точное представление о характере элементарных частиц.
В результате серии опытов был определен отрицательный заряд электронов. При этом имелась информация о нейтральном заряде атомов. Томсон выдвинул предположение о наличии некого источника положительного заряда в атоме, что позволяет компенсировать отрицательный заряд электронов. Английским физиком было выдвинуто несколько вероятных механизмов взаимодействия частиц, находящихся внутри атома:
- электрон с отрицательным зарядом присоединяется к частице с положительным зарядом и перемещается вместе с ней;
- электроны совершают вращательные движения вокруг центральной области положительного заряда, который характеризуется такой же величиной, что и все электроны;
- электроны занимают область пространства, являющуюся самостоятельным однородным положительным зарядом.
Ученый остановился на третьем варианте, который казался ему наиболее вероятным, отражающим структуру атомов. Публикация модели атома Томсона состоялась в 1904 году в мартовском выпуске издания Philosophical Magazine. Журнал пользовался авторитетом в Британии.
Мнение автора заключалось в том, что атомы элементов включают в себя определенное количество отрицательно наэлектризованных корпускул или электронов, которые заключены в сферу равномерной положительной электризации. Тем самым, ученый отказался от предшествующей своей теории о «туманном атоме», согласно которой частицы состояли из нематериальных вихрей.
Научное сообщество проявило большой интерес к публикации Томсона. Однако гипотеза столкнулась с критикой со стороны многих авторитетных физиков по причине отсутствия прочных доказательств. С другой стороны, рассматриваемая модель атома полностью отвечала представлениям и результатам экспериментов, которые были известны в то время.
Только в 1911 году была представлена более точная модель атома Резерфорда. Отличие от модели Томсона заключается в том, что, согласно представлениям Резерфорда, положительный заряд расположен в малой области атома, а компенсирующие электроны окружают его. К такому утверждению ученый пришел в результате экспериментов по бомбардировке атомов. В дальнейшем данная модель рассматривалась в качестве планетарной модели атома по Резерфорду.
Как описывал атом Томсон, почему модель назвали «Пудинг с изюмом»
Томсон был известен, как проницательный и практичный ученый. Основываясь на известных экспериментальных данных, он выдвинул гипотезу об атомной модели. Предположение о том, что объем заряда положительный, является отражением научного подхода Томсона к открытию, которое стало руководством к действию для дальнейших экспериментов.
Исходя из теории, стабилизация орбит электронов внутри атомной модели Томсона объясняется воздействием возрастающей силы притяжения на электрон, удаляющийся от центра положительно заряженной сферы или облака. Данное воздействие способствует возвращению электрона, что обусловлено законом Гаусса, подтверждающим более высокую концентрацию положительного заряда во внутренней области сферы.
Рассматриваемая модель предполагает свободное вращение электронов по кольцам, дополнительно стабилизированным, благодаря взаимодействию электронов между собой. С помощью спектроскопических значений объяснялись энергетические различия между отдельными кольцевыми орбитами.
По представлениям тех времен, расположение электронов в сфере с положительным зарядом напоминало изюм в пироге или фруктовые кусочки в сливовом пудинге. В связи с этим концепция приобрела название «пудинговой» модели атома.
Плюсы и минусы теории
Модель Томсона является объяснением излучения атомов. Однако весь комплекс эмпирических данных по спектрам атома не был подтвержден в этой модели. Формулы определенных химических элементов описали их спектры, но противоречили рассматриваемой модели. Таким образом, с помощью модели Томсона не получилось объяснить дискретный характер, которым обладают спектры атомов.
Проблема также заключалась в описании устойчивости атома. Представленная модель не могла охарактеризовать рентгеновское и гамма-излучения, которые испускают атомы. Кроме того, отсутствовали пояснения относительно определения размеров атома. Модель противоречила опытам, направленных на изучение того, как распределяется положительный заряд в атоме. Спустя некоторое время после создания модель Томсона признали ошибочной.
В настоящее время рассматриваемая модель имеет историческое значение и, несмотря на несостоятельность, является важным элементом в цепочке развития научных знаний о строении вещества. В качестве еще одного достоинства модели атома Томсона можно отметить ее простоту. Благодаря этому преимуществу, гипотезу удалось опровергнуть и продвигать науку дальше.
Дилемма несоответствия, дальнейшее развитие
С увеличением объема экспериментальных данных научное сообщество убеждалось в том, что сущность модели атома Томсона не соответствовала действительности. Попытки ученого усовершенствовать выдвинутую гипотезу не увенчались успехом. Томсону не удалось объяснить некоторые из ключевых спектральных линий, которые были выявлены опытным путем при исследовании состава нескольких элементов.
В 1909 году Ганс Гейгер и Эрнест Марсден под кураторством профессора Эрнеста Резерфорда поставили опыты над тонким золотым листом. Схема эксперимента заключалась в рассеивании альфа-частиц на фольге из золота. Полученные данные не оправдали ожидания. В 1911 году Резерфорд по итогу длительных размышлений представил миру собственную концепцию, которая затем получила название «модель атома Резерфорда».
Ученый предположил, что в центральной области атомов золота находится очень маленькое ядро, обладающее мощным положительным зарядом, что позволяет удержать порядка ста электронов.
Сразу после публикации гипотезы Резерфорда было выдвинуто предположение ученым Антониусом Ван ден Бруком о равенстве атомного номера элемента общему количеству единиц заряда, которые присутствуют в его ядре. В 1913 году Генри Мозли предоставил нужную информацию, доказывающую теорию Ван ден Брука. Было установлено соответствие эффективного ядерного заряда атомному номеру.
Исследование легло в основу характеристики полуклассической модели атомов, созданной Нильсом Бором в 1913 году. Данная модель напоминает то, как взаимодействуют Солнце и планеты в Солнечной системе, но при наличии квантовых ограничений.
Благодаря модели атома Томсона, ядерная физика получила стремительное развитие. Концепцию «сливового пудинга» с одним электроном использовал физик Артур Эрих Хаас в 1910 году, чтобы оценить численное значение постоянной Планка и определить боровский радиус атомов водорода.
Хаас опубликовал работу на три года раньше, чем были представлены выводы Нильса Бора. Важно заметить, что боровская модель обеспечивает достаточно точные прогнозы для атомных и ионных систем, имеющих один эффективный электрон. С помощью теории «пудинга» можно рассчитать оптимальное распределение идентичных точечных зарядов на единичной сфере, которую называют проблемой Томсона.
Физическая система, отраженная в проблеме Томсона, представляет собой частный случай одной из восемнадцати математических задач без решения, которые предложил математик Стив Смейл - «распределение точек на двумерной сфере». Проблема Томсона – это естественное следствие модели «пучкового пудинга» в отсутствие равномерного положительного фонового заряда.
Электростатическое взаимодействие электронов, которые ограничены с помощью сферических квантовых точек, идентично их обработке в атомной модели Томсона. Классическая задача подразумевает моделирование квантовой точки как простой диэлектрической сферы со свободными или избыточными электронами, а не однородной сферы с положительным зарядом, которая описана в модели «пучкового пудинга».
Заметили ошибку?
Выделите текст и нажмите одновременно клавиши «Ctrl» и «Enter»
Нашли ошибку?
Текст с ошибкой:
Расскажите, что не так