Молекулярная физика: основные формулы
Что такое молекулярная физика
Молекулярная физика — раздел физики, который изучает физические свойства тел на основе рассмотрения их молекулярного строения.
Свойства любого вещества диктуются особенностями его молекулярного строения. От индивидуальных характеристик строения молекулярной решетки, изменения межмолекулярных связей под воздействием факторов окружающей среды и времени их контакта зависят закономерности тех или иных процессов.
На физические свойства тел могут влиять давление, температура, электромагнитные поля. В результате этого первоначальные свойства предмета частично либо полностью видоизменяются. На практике, выбирая тот или иной состав вещества, обязательно учитывают его поведение при различных условиях эксплуатации: смену фазового состояния, появление поверхностных явлений и т.п.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Дать объяснение кардинальному либо частичному качественному изменению свойств можно только с позиции описания их макроскопических характеристик, вытекающих из микроскопического строения. Проявление законов межмолекулярных связей дают пояснение поведению тел при любых условиях.
Основные величины молекулярной физики и соотношения между ними
В основе физики, основывающейся на молекулярных особенностях, лежат величины, от них зависящие. Схематически их можно охарактеризовать следующим образом:
- Масса вещества (m).
- Объем (V).
- Плотность (ρ).
- Концентрация (n).
- Число частиц вещества (N).
Основные величины молекулярной физики взаимосвязаны друг с другом посредством следующих математических выражений:
\(\rho=m\div V\)
а значит \(\rho m=\rho\times V\\\)
Если N — число частиц вещества, а mo — масса каждой из них, то общая масса равна:
\(m=N\times mo\\\)
Концентрацию вещества можно высчитать по формуле:
\(n=N\div V\left\{\right\}\\\)
При умножении mo на N получится плотность ρ.
Формулы с пояснениями и обозначениями, к каким процессам применимы
В зависимости от условий окружающей среды вещества могут переходить из одного агрегатного состояния в другое:
- твердое;
- жидкое;
- газообразное.
Исходя из этого, оно проявляет различные свойства, изучение которых — задача молекулярной физики. Ее главной основой является молекулярно-кинетическая теория, рассматривающая тепловое движение молекул и атомов.
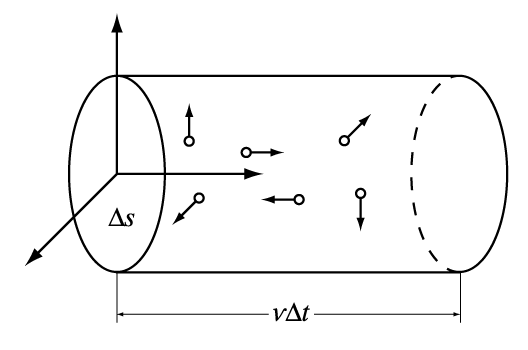
Основное уравнение молекулярно-кинетической теории идеального газа
Основополагающими моментами молекулярно-кинетической теории являются следующие:
- любое вещество имеет молекулярно-атомное строение;
- внутренние микрочастицы находятся в постоянном, хаотическом движении;
- они способны взаимодействовать друг с другом.
Атомы, как и молекулы, электрически нейтральны, однако способны становиться положительными или отрицательными ионами, получая элетрозаряд. Тогда они называются катионами и анионами.
Если в обычном состоянии молекулы движутся хаотично (беспорядочно), то с возрастанием температуры увеличивается их кинетическая энергия, они разлетаются, а само вещество постепенно переходит в газообразную стадию. При низких температурах, напротив, молекулы конденсируются, а вещество переходит в жидкую или твердую форму.
Характер движения молекул в различных фазах различается. Если в твердой фазе они колеблются вокруг зафиксированных центров, то в жидкостях более свободны и могут осуществлять движение по всему объему. Именно этой особенностью вызывается такое свойство, как текучесть.
Для газообразного состояния характерно значительное превышение размеров расстояния между молекулами, чем их собственные габариты. Поэтому силы взаимодействия между ними невелики. Каждая микрочастица движется беспорядочно, пока не столкнется с себе подобной или стенкой сосуда. Это свойство вызывает способность газа расширяться и распространяться по всему объему сосуда.
Идеальный газ — теоретическая модель, широко применяемая для описания свойств и поведения реальных газов при умеренных давлениях и температурах.
Математическое выражение основного уравнения молекулярно-кинетической теории выглядит так:
\(p=1⁄3n\times mo\times V2 кв\)
Где p — давление газа, n — концентрация молекул в единице объема, mo — масса одной молекулы, Vкв — среднеквадратичная скорость молекулы.
Теоретическая суть уравнения заключается в определении зависимости между макротелом (газ, заключенный в сосуд) и его микропараметрами (характер движения молекул и атомов).
Молекула, сталкиваясь со стенкой сосуда, меняет свой импульс, поскольку не только она передает энергию стенке, но и получает противоположно направленный импульс. Это явление объясняют второй и третий законы Ньютона. Сумма всех ударов молекул о стенку создает давление газа.
Уравнение Менделеева-Клапейрона
Из постулатов молекулярно-кинетической теории вытекает уравнение состояния идеального газа:
\(p\times V=v\times R\times T\)
Где p — давление, V — объем, v — скорость движения частиц, R — универсальная газовая постоянная, равная 8,31 Дж/(моль∙К), T — температура
Это уравнение состояния идеального газа. Его открытие принадлежит Клайперону.
Первоначально оно было сформулировано для одного моля газообразного вещества, позднее Менделеев установил его справедливость для большего количества молей.
Данное уравнение подразумевает определение параметров идеального газа, находящегося при нормальных условиях (температуре 273 К и давлении 1 атм).
Исходя из анализируемого равенства, известные параметры состояния идеального газа всегда помогут найти искомую величину. В то же время изменение любого из них вызовет коррекцию всех остальных.
Законы физиков Бойля, Гей-Люссака и Шарля
Физические законы, которые объясняют поведение идеального газа и дают возможность определить заданные показатели, носят имена своих открывателей. В зависимости от того, о чем идет речь в задаче, важно правильно выбрать закон, отражающий нужный критерий. Перед тем, как перейти к их характеристике, нужно обозначить следующие термины:
- парциальное давление — P, оказываемое газом, если бы в смеси не присутствовали другие компоненты;
- изотермический процесс — условия с постоянной температурой;
- изобарный процесс — условия с постоянным давлением;
- изохорный — с постоянным объемом.
Если в задаче идет речь о количестве молекул применяется закон Авагадро, о смеси газов — закон Дальтона, при постоянном объеме газа — закон Шарля, изобарном процессе — Гей-Люссака, изотермическом — Бойля-Мариотта. При постоянной массе газа действует универсальный закон Клайперона.
Следствием уравнения Клайперона-Менделеева является газовый закон, открытый в 1662 году Р.Бойлем и параллельно — Э.Мариоттом (1676 г). Он гласит, что при постоянных массе и температуре величина, равная произведению давления газа на его объем остается неизменной.
Существует и другая, параллельная первой, формулировка: если температура газа постоянна, то давление его определенной массы обратно пропорционально объему.
Математическая запись выглядит следующим образом:
\(p1\div p2=V2\div V1\)
Закон Гей-Люссака гласит, что объем газа прямо пропорционален его абсолютной температуре. Обязательное условие для данного выражения — постоянное давление (процесс изобарный). Закон был открыт в 1802 году.
В качестве следствия из этого закона в курсе физики приводится заключение, что при постоянных массе и давлении газа соотношение объема и температуры газа остается постоянной величиной.
Для закона Гей-Люссака необходимо соблюдение изобарности процесса и постоянстве массы.
Закон Шарля называют вторым законом Гей-Люссака. В нем идет речь о соотношении температуры и давления идеального газа при постоянном объеме. Закон был открыт в 1787 году Шарлем. Уточнен в 1802 году Гей-Люссаком.
Формулировка закона Шарля: при фиксированных массе и объеме идеального газа давление прямо пропорционально абсолютной температуре идеального газа.
Закон имеет теоретическое подтверждение, поскольку мера средней кинетической энергии вещества — это температура. При ее увеличении частицы сильнее ударяются о стенку сосуда и количество ударов создает более высокое давление.
В качестве следствия из этого закона часто применяется следующее понятие: при постоянных массе и объеме идеального газа отношение его давления к температуре является постоянным. Обязательное условие — изохорность процесса.
Для решения задач с помощью газовых законов температура переводится из градусов Цельсия в Кельвины.
Закон Дальтона
Если сосуд заполняется не чистым газом, а смесью нескольких компонентов, то для определения давления на стенки применяется закон Дальтона.
Согласно закону Дальтона, общее давление будет равно сумме давлений каждого из компонентов смеси.
В этом законе вводится термин «парциальное» давление, т.е. то, которое производил бы один из компонентов, если бы был единственным.
Математическое выражение выглядит следующим образом:
p=p1+p2+p3+...pn
Обязательным условием действия этого закона является отсутствие химического взаимодействия между входящими в состав газовой смеси элементами.
Заметили ошибку?
Выделите текст и нажмите одновременно клавиши «Ctrl» и «Enter»
Нашли ошибку?
Текст с ошибкой:
Расскажите, что не так