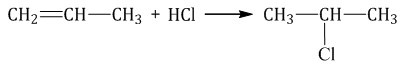Способы получения алкенов и их основные химические свойства
Что такое алкены, где применяются
Алкены (олефины) — непредельные углеводороды, содержащие в структуре молекулы одну двойную связь.
Второе название — олефины —алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров — масел.
Общая формула
\(C_nH_{2n}\)
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Физические свойства
- обладают резким запахом;
- отсутствует цвет;
- нерастворимы в воде.
Алкенам присущи реакции присоединения, проходящие по двойной связи.
Применение
- производство пластмасс, пакетов, пленок, упаковок,
- использование в получении полимеров, эфиров, спирта, каучука.
Уравнения реакций, характеризующих химические свойства алкенов
- Гидрирование.
\(СН_3-СH=CH_2\;+\;H_2\;\xrightarrow{Pt}CH_3-CH_2-CH_3\)
В данной реакции используются катализаторы — платина или никель. - + галогены.
\(СН_3-СH=CH_2\;+\;Cl_2\;\xrightarrow{CCl_4}CH_3-CHCl-CH_2Cl\)
В реакции участвует органический растворитель. - + галогенводороды.
\(СН_3-СH=CH_2\;+\;HBr\;\rightarrow CH_3-CHBr-CH_3\) - + вода.
\(СН_3-СH=CH_2\;+\;H_2O\;\rightarrow CH_3-CHOH-CH_3\)
Способы получения алкенов
- Крекинг алканов.
\(СН_3-СH_2-CH_2-CH_2-CH_3\rightarrow CH_3-CH=CH_2\;+\;CH_3-CH_3\) - Дегидрогалогенирование моногалогеналканов.
\(СН_3-СHBr-CH_3\;+\;KOH_{спирт.р.}\;\rightarrow CH_3-CH=CH_2\;+KBr\;+\;H_2O\)
Щелочь должна быть в спиртовом растворе. - Дегидратация спиртов.
\(СН_3-СHOH-CH_3\;\xrightarrow{t^\circ,\;H_2SO_4}\;CH_3-CH=CH_2\;+\;H_2O\)
Используем водоотнимающий реагент. - Дегидрирование алканов.
\(СН_3-СH_2-CH_3\;\xrightarrow{t=500^\circ C,\;Cr_2O_3}СH_3-СH=СH_2\;+\;H_2\) - Дегалогенирование дигалогеналканов.
\(СН_3-СHBr-CH_2Br\;+\;Mg\;\rightarrow\;CH_3-CH=CH_{2\;}+\;MgBr_2\)
Реакции присоединения алкенов
Реакции присоединения галогенводородов происходят согласно правилу Марковникова.
Правило Марковникова гласит, что при взаимодействии несимметричных алкенов или алкинов со сложным веществом вида «HX» (на месте Х чаще всего стоит атом галогена или гидроксильная группа) водород присоединяется к более гидрогенизированному, а атом Х — к менее гидрогенизированному атому углерода, стоящему при двойной связи.
Исключением является реакция бромоводорода с участием пероксида водорода (перекисный эффект Хараша).
При присоединении хлороводорода HCl к пропилену атом водорода преимущественно присоединяется к атому углерода группы \(СН_2=\), поэтому преимущественно образуется 2-хлорпропан.
Заметили ошибку?
Выделите текст и нажмите одновременно клавиши «Ctrl» и «Enter»
Нашли ошибку?
Текст с ошибкой:
Расскажите, что не так