Химические и физические свойства фенолов
Что такое фенолы
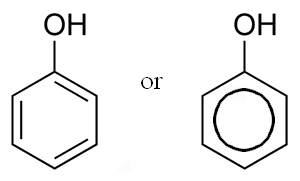
Из курса химии известно, что спирты представляют собой гидроксид-соединения, для которых характерно соединение группы ОН с алифатическим углеводородным радикалом R-OH. В том случае, когда гидроксогруппа ОН обладает связью с бензольным кольцом, полученное вещество можно причислить к фенолам. Руководствуясь полученными данными из исследований химического соединения, целесообразно сформулировать понятие для этого вещества.
Фенолами называют соединения органического происхождения в ароматическом ряду с молекулами, обладающими связями между гидроксильными группами OH− и углеродными атомами ароматического кольца.
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
Источник: ru.wikipedia.org
Рассматриваемые вещества встречаются в природном мире. Однако известность и широкое распространение получили соединения, которые синтезированы в лабораторных и промышленных условиях. Стоит отметить, что такие материалы незаменимы в области производства химической продукции, пластика, медицинских товаров.
Фенолы отличаются сильными токсичными способностями. Соединения характеризуются повышенной степенью устойчивости. Вещества обладают высокой проникающей способностью. Через кожные покровы и дыхательные органы фенолы попадают в организм. Процесс сопровождается отравлением. Исходя из перечисленных свойств, вещество причисляют к группе высокоопасных. По этой причине использование фенолов регламентировано строгими правилами, что требуется с целью предотвращения травм и других опасных последствий для здоровья, соблюдения строгих правил безопасности.
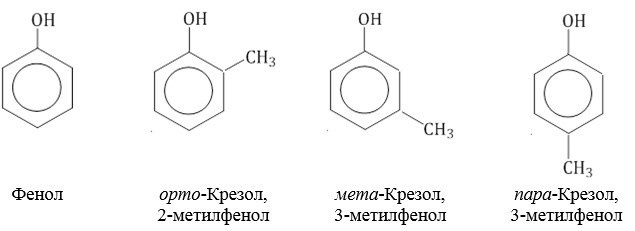
Классификация фенолов:
- Для фенолов с единственной группой ОН характерна запись в виде \(C_{n}H_{2n-7}OH или C _{n}H_{2n-6}O\).
- Фенолы, у которых пара групп ОН, с общими формулами \(C_{n}H_{2n-8}(OH)_{2} или C_{n}H_{2n-8}O_{2}\).
Источник: chemege.ru
К химическим веществам люди давно относятся с некоторой настороженностью и соблюдают меры безопасности при проведении экспериментальных опытов и реализации разнообразных технологических процессов. К примеру, соль, которую все повара используют в кулинарии, представляет в определенных дозах, а именно, свыше 3 г на 1 кг веса, смертельную опасность. А другие соединения, признанные ядами, в строго отмеренных концентрациях обладают положительным эффектом, действуя как лекарственные средства. К таковым можно отнести фенол, то есть карболовую кислоту.
Химические свойства фенола
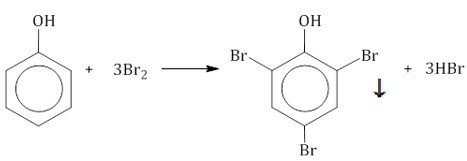
За счет присутствия ОН-группы в бензольном кольце фенол приобретает особое свойство достаточно просто по сравнению с бензолом участвовать в химических процессах замещения в ароматическом кольце. Рассмотрим реакцию галогенирование. В этом случае, когда температурный режим соответствует комнатному, при отсутствии катализатора фенол реагирует на бромную воду. В результате взаимодействия выпадает осадок белой окраски 2,4,6-трибромфенола. Этот процесс можно описать как качественную реакцию на присутствие фенола.
Источник: chemege.ru
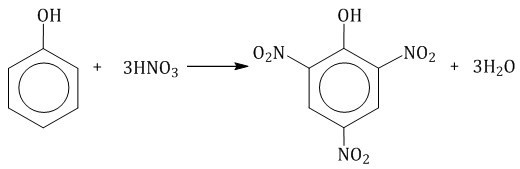
Фенол участвует в реакциях нитрования. К примеру, если на вещество оказывает воздействие 20% азотная кислота, то оно трансформируется в смесь из орто- и пара-нитрофенолов. Такой результат характерен для взаимодействия фенола с излишком концентрата азотной кислоты. Рассматриваемый процесс сопровождается образованием 2,4,6-тринитрофенола, то есть пикриновой кислоты.
Источник: chemege.ru
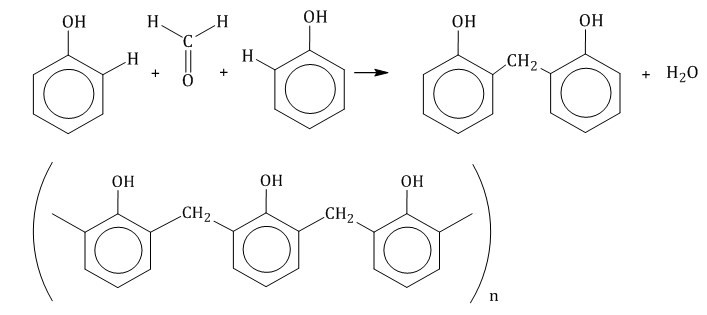
В результате химического контакта фенола и формальдегида формируются соединения в виде фенолоформальдегидных смол.
Источник: chemege.ru
Фенол участвует в реакциях с хлоридом железа (III). Результатом подобного химического взаимодействия является образование комплексных соединений железа. В процессе смесь приобретает сине-фиолетовую окраску. Таким образом, реализована качественная реакция на фенол.
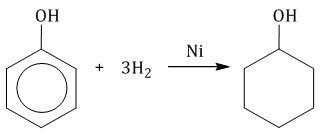
Фенол участвует в восстановительных реакциях. В процессе гидрирования фенола водород присоединяется к ароматическому кольцу. Продуктом химического взаимодействия по описанной схеме является циклогексанол, то есть вторичный циклический спирт.
Источник: chemege.ru
Если вещества под названием фенолы имеют природное происхождение, то такие соединения играют роль антиоксидантов, полифенолов. За счет подобного состава растительные организмы приобретают уникальные целебные свойства, которые высоко ценят в медицине. Опасно путать данные виды фенолов с синтетическими соединениями. Искусственно полученные вещества являются ядами, которые при контакте с кожными покровами провоцируют ожоговые реакции, а также отравляют организм человека.
Физические свойства
В распространенных случаях фенолы с одним атомом при условиях, соответствующих норме, представлены кристаллами, не обладающими окраской. Такие вещества плавятся при небольшом температурном режиме и имеют специфический запах. Степень растворимости в воде в случае фенолов невысока. С другой стороны, рассматриваемые вещества легко растворить в растворителях органического происхождения.
Фенолы оказывают токсичный эффект. Если вещество поместить в воздушное пространство, то можно наблюдать, как со временем в процессе окисления кристаллов оно приобретает более темную окраску. Карболовую кислоту, которую также относят к категории фенолов, при нагреве до 66°C и выше достаточно просто смешать с водой, независимо от выбранного соотношения.
Фенол имеет кристаллическую структуру с характерными образованиями в виде игл. Соприкасаясь с кожными покровами, вещество наносит повреждения эпидермису, включая ожоги. Если человек какое-то время дышит воздухом с определенным содержанием фенола, то нервной системе организма наносится значительный урон, что сопровождается серьезными проблемами с дыхательными органами и сердцем. При работе с фенолом в лабораторных условиях специалисты применяют специальные средства защиты. Манипуляции с веществом осуществляют в плотных перчатках из материала, который устойчив к агрессивным средам, при функционирующей вытяжке.
Кислотные свойства
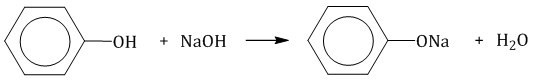
Осуществима химическая реакция фенолов с гидроксилами щелочных и щелочноземельных металлов. Стоит отметить, что подобное взаимодействие не характерно для спиртов. Результатом процесса является образование солей, то есть фенолятов. В качестве типичного примера такой реакции можно рассмотреть контакт фенола и гидроксида натрия, что приводит к формированию фенолята натрия.
Источник: chemege.ru
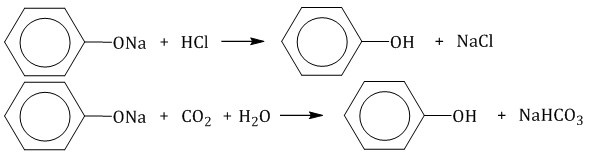
В процессе постановки химических опытов важно учитывать, что фенол представляет собой более слабую кислоту в сравнении с угольной или соляной. Получение вещества допустимо, когда из фенолята вытесняют фенол с применением соляной или угольной кислоты.
Источник: chemege.ru
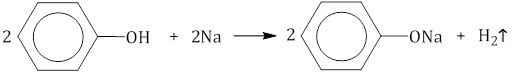
Образование фенолятов является следствием реакции фенолов с активными металлами, включая щелочные и щелочноземельные. В процессе реализации функции химического взаимодействия поведение фенолов аналогично кислотам. Примером такого процесса служит реакция фенола на натрий. В результате образуется основа из фенолята натрия, и выделяется водород по уравнению:
Источник: chemege.ru
Заметили ошибку?
Выделите текст и нажмите одновременно клавиши «Ctrl» и «Enter»
Нашли ошибку?
Текст с ошибкой:
Расскажите, что не так